TÜM BEŞERİ TIBBİ ÜRÜNLER İÇİN NİTROZAMİN RİSK DEĞERLENDİRMELERİ GEREKLİDİR – HAZIRLIKLI MISINIZ? Beşeri tıbbi ürünlerle uğraşıyorsanız, tüm ürünleriniz için nitrozamin risk değerlendirmesi yapmalısınız. Risk değerlendirmelerinin kendilerinin ibraz edilmesine gerek yoktur, ancak sonucun (risk tanımlanmış veya risk tanımlanmamış) yetkili makamlara bildirilmesi gereklidir. Kimyasal içerikli ilaçlar için son tarih 31 Mart 2021 Biyolojik ilaçlar için son tarih...
Tecrübeli ekibimizle tesisinizdeki bilgisayarlı sistemlerin validasyonu ile ilgili ihtiyaçlarınızı kaşılayacak projeler gerçekleştiriyoruz. Bilgisayarlı sistemler envanterinin oluşturulması Bilgisayarlı sistemlerin sınıflandırılması Bilgisayarlı sistemlerde eksiklik (GAP) analizi GxP ve veri bütünlüğü risklerinin değerlendirilmesi Bilgisayarlı sistemlerin GAMP5 yaklaşımına göre validasyonu Risklerin iyileştirilmesi ve elimine edilmesi için aksiyonların planlanması Risklerin iyileştirilmesi ve elimine edilmesi için aksiyonların planlanması Bilgisayarlı sistemler için...
Teknoloji Transferi sistematik olmak zorundadır ve Ar & Ge aşamasında itibaren elde edilen dokümante edilmiş tüm bilgi ve deneyimlerin uygun, sorumluluk alabilecek ve yetkili taraflara devrini zorunlu tutmaktadır. Teknoloji Transferinde tüm parametrelerin eksiksiz olarak yerine getirilebilmesi için öncelikle Teknolojiyi Gönderen Birim ve Teknolojiyi Alan Birim arasındaki koordinasyon ve işbirliğinin maksimum önem taşıdığının tüm taraflarca benimsenmesi...
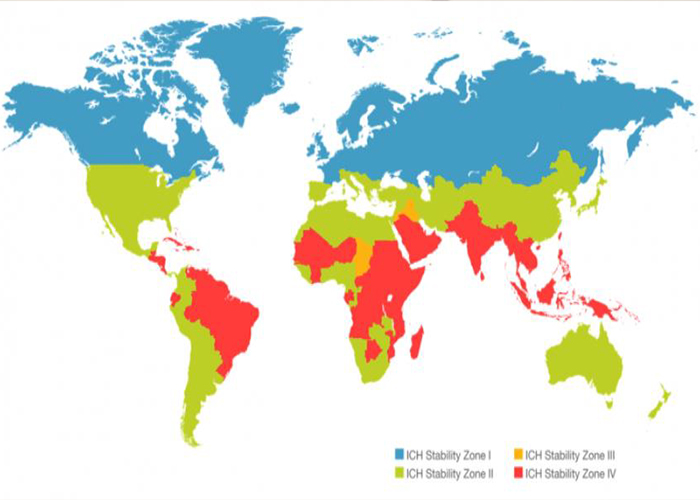
Stabilite çalışmaları farmasötik ürünlerin raf ömürlerinin belirlenmesi için yapılması gereken en temel çalışmalardan biridir. Bu çalışmalar öncelikle ARGE aşamasında ARGE bölümleri tarafından gerçekleştirilmektedir. Stabilite çalışmalarının hangi iklim bölgeleri için hangi detayda yapılması gerektiğinin detaylıca işlendiği eğitim kapsamında farklı saklama koşulları için otorite gereklilikleri ve izleme süreçleri açıklanmaktadır. Otorite talepleri doğrusunda hangi detayda çalışma yapılacağı ve...
Elemental safsızlıklar hiçbir terapötik fayda sağlamayan ve hastalara zarar verme potansiyeline sahip metalik elementlerdir, bu nedenle hastaların güvenliğini sağlamak için sıkı bir şekilde takip edilmeleri gereklemtedir. Toplum sağlığını korumak için: Uluslararası Uyumlaştırma Konseyi (ICH) tarafından yayınlanan Elemental Safsızlıklar Kılavuzu ICH Q3D 1 Ocak 2018’den bu yana AB’ de ve US’ de tüm yeni pazarlama yetkileri...
Metot validasyonu, kaliteli analitik verinin oluşturulması ve metodun belirli bir uygulama için uygun veriler sağlayabildiğine dair kanıtların sağlanması için izlenen önemli bir süreçtir. Analitik Metodun performansı, yeterliliği ve amaca uygunluğu Analitik Metot Validasyonu ile garanti edilir. Bu eğitim hem analitik metot validasyonunun nasıl planlanacağına, yapılacağına ve raporlanacağına yönelik bilgileri ve hem de, validasyon verilerini yorumlamak...
Çok sayıda ürünün aynı üretim yerinde ve aynı ekipmanlar kullanılarak üretilmesi gerekliliği nedeni ile ürünlerin birbirlerini kontamine etmeleri ve bu kontaminasyon neticesinde üretilen bir sonraki ürünü kullanan hastanın bu kontaminasyondan negatif olarak etkilenmesi çok büyük bir olasılıktır. Bu tür tesisler için yapılması gereken ve otoritelerin de beklediği en temel yaklaşım firmaların etkin temizlik prosedürlerinin mevcut...
GMP’nin en temel gerekliliği olan Veri Bütünlüğü son yıllarda artan önemi ile hem otorite denetimlerinin ve de tedarikçi denetimlerinin olmazsa olmaz konularının başında gelmektedir. Peki “Veri Bütünlüğü neden bu kadar önemlidir?” Ürün kalitesinin ve hasta sağlığının korunması güvenli, kaliteli ve kullanım amacına uygun ürünlerin üretilmesi ile sağlanır. Bunun garanti edilmesi için ürün yaşam döngüsü boyunca...
İyi Dağıtım Uygulamaları / İyi Üretim ve Dağıtım Uygulamaları Farmasötik Endüstri için ürün kalitesinin başından sonuna korunmasını garanti eden önemli bir bileşen olması açısından çok büyük önem arz etmektedir. Farmasötik ürünlerin üretildikten ve satış için serbest bırakıldıktan sonra kullanıcı olan hastaya ulaşana kadar geçen süre zarfında kalitelerinin eksiksiz bir şekilde korunmasının sağlanması için iyi depolama...
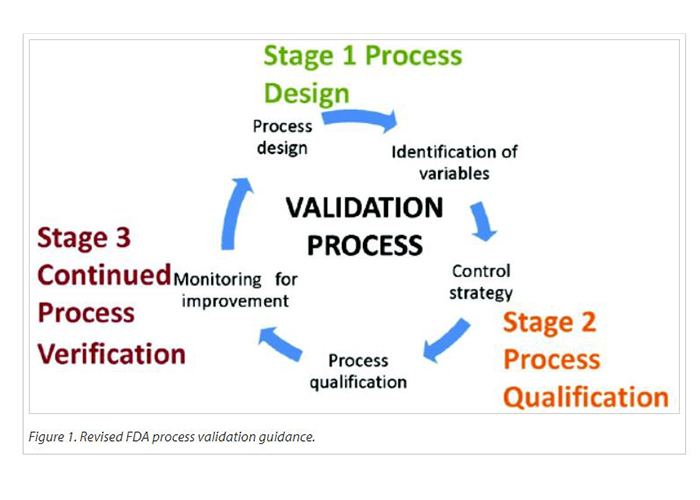
2011’de FDA tarafından ve 2014’de EMA tarfından yayınlanmış olan yaşam döngüsü boyunca proses doğrulama kılavuzları ile tüm otoriteler tarafından kabul gören 3 parti ile valide etme yaklaşımı yerini 21. Yüzyılın bilim ve risk temelli proses validasyonu uygulamalarına bırakmıştır. Bu sayede ürün geliştirmeden başlayıp, teknoloji transferi ve ticari üretim ile devam eden ürün yaşam döngüsü sırasında...